

هیدرازین چینی ۵۵%
شرکت جهان شیمی واردکننده هیدرازین چینی ۵۵% با کیفیت عالی و مناسب ترین قیمت در بشکه های ۲۰۰ کیلویی می باشد. جهت خرید و استعلام قیمت فروش هیدرازین ۵۵% با ما تماس حاصل فرمایید.
هیدرازین چیست و چه کاربردی دارد؟
هیدرازین یک ترکیب معدنی با فرمول شیمیایی N2H4 و مایعی بی رنگ و قابل اشتعال با بوی آمونیاک است. هیدرازین بسیار سمی است و به طور خطرناکی ناپایدار است مگر اینکه به صورت محلول استفاده شود.
این ماذه شیمیایی عمدتا به عنوان ماده کف ساز در تهیه فوم های پلیمری مورد استفاده قرار می گیرد، اما کاربردهای دیگر آن شامل پیش ساز کاتالیزورهای پلیمریزاسیون، کاربرد در داروسازی و کشاورزی می باشد.
این ترکیب در سوخت های مختلف موشکی و برای تهیه پیش سازهای گازی مورد استفاده در کیسه های هوا استفاده می شود. در نیروگاه های هسته ای و معمولی برای حذف اکسیژن جهت کنترل غلظت اکسیژن محلول، جهت کاهش خوردگی تجهیزات استفاده می شود.
هیدرازین یک بلوک ساختاری برای بسیاری از ترکیبات هتروسیکلیک از طریق تراکم الکتروفیل های دو عملکردی و یک ماده کاهنده مناسب است زیرا فرآورده های جانبی آن معمولا گاز ازت و آب هستند. بنابراین به عنوان یک آنتی اکسیدان، پاک کننده اکسیژن و مهار کننده خورندگی در دیگ های بخار و سیستم های گرمایشی استفاده می شود.
این ماده همچنین برای احیاء نمک ها و اکسیدهای فلزی به فلزات خالص در آبکاری نیکل و استخراج پلوتونیوم از ضایعات راکتور هسته ای کاربرد دارد.
تقاضای بازار جهانی برای هیدرازین ۸۰ تا ۹۰ هزار تن در سال است که تقریباً ۳۲٪ آن برای تولید سموم دفع آفات، ۳۳٪ برای تولید کف، ۲۰٪ برای تصفیه آب و ۱۵٪ برای سایر مقاصد مصرف می شود. پیش بینی می شود که تقاضا برای این ماده در آینده به طور مداوم رشد خواهد کرد، با اینحال اگرچه تقاضا در کشورهای پیشرفته کاهش می یابد ولی در کشورهای در حال توسعه، به ویژه کشورهای آسیایی، به سرعت در حال رشد است.

هیدرازین چینی ۵۵%
کاربردهای هیدرازین
- به عنوان سوخت محرک در فضاپیماها استفاده می شود. از دیگر کاربردهای این ماده می توان به کاهش غلظت اکسیژن محلول و کنترل pH آب در دیگ های بخار اشاره کرد. هیدرازین همچنین برای سوخت رسانی به واحدهای برق اضطراری استفاده می شود.
- این ماذه شیمیایی پیش ماده داروهای مختلف و سموم دفع آفات است. اغلب این کاربردها شامل تبدیل این ماده به حلقه های هتروسیکلی مانند پیرازول ها و پیریدازین است. نمونه هایی از مشتقات فعال زیستی تجاری هیدرازین عبارتند از: سفازولین، ریزاتریپتان، آناستروزول، فلوکونازول، دیکلوبوترازول و هیدرازین سولفات.
- ترکیبات هیدرازین می توانند به عنوان عناصر فعال در ترکیب با سایر مواد شیمیایی کشاورزی مانند حشره کشها، مایت و کرم کش ها، قارچ کشها، ضد ویروسها، چسب های جذب کننده ، علف کش ها یا تنظیم کننده های رشد گیاه مؤثر باشند.
- هیدرازین یک واسطه در اکسیداسیون بی هوازی (فرایند آناموکس) است. این ماده توسط برخی مخمرها و باکتری های آزاد آناموکس اقیانوس نیز تولید می شود. حتی محبوب ترین قارچ خوراکی – قارچ های تکمه ای – مشتقات آلی هیدرازین از جمله آگاریتین و ژیرومیترین را تولید می کند.
- خواص فیزیکی این ماده شبیه آب است ولی هیدرازین بی آب، یک مایع روغنی بی رنگ و با بوی شبیه آمونیاک می باشد. این ماده در حین تقطیر منفجر خواهد شد اگر مقداری هوا در فرآیند موجود باشد.
ساختار لوویس هیدرازین
ساختار لوویس و ساختار نقطه الکترونی، تصویری از فرمول مولکولی یک ترکیب شیمیایی به همراه الکترون های آن است که به صورت نقطه نشان داده می شوند. این ساختارها به افتخار شیمیدان آمریکایی گیلبرت نیوتن لوویس که آنها را در سال ۱۹۱۶ معرفی کرد، نامگذاری شده اند.
ساختارهای لوویس پیوند شیمیایی بین اتم های مختلف یک مولکول و همچنین تعداد جفت های تک الکترون موجود در آن مولکول را نشان می دهند. می دانیم که فقط الکترون های ظرفیت یک اتم در پیوندهای شیمیایی شرکت می کنند تا قاعده اکتت یا هشتگانه آن اتم را برآورده کنند. در مورد N۲H۴ نیتروژن دارای پنج الکترون است در حالی که هیدروژن فقط یک الکترون ظرفیت دارد.
در این ترکیب شیمیایی باید به این نکته توجه داشت که قانون اکتت در مورد هیدروژنی که با دو الکترون پایدار می شود، صدق نمی کند. بنابراین، هر اتم نیتروژن یک پیوند منفرد با دو اتم هیدروژن و اتم نیتروژن دیگر تشکیل می دهد و قاعده هشتگانه برای همه اتم های شرکت کننده را برآورده می کند.
قطبیت هیدرازین
وجود دو بار یا قطب مخالف در یک مولکول به عنوان قطبیت شناخته می شود. دلیل ایجاد این بارها در یک مولکول، اختلاف الکترونگاتیوی است که بین اتم های سازنده آن مولکول وجود دارد. در مورد مولکول هیدرازین می دانیم که دو اتم نیتروژن در یک صفحه قرار دارند و همچنین تفاوت الکترونگاتیوی بین این دو اتم وجود ندارد بنابراین پیوند بین آنها غیر قطبی است.
قطبیت مولکول N۲H۴ به دلیل اختلاف الکترونگاتیوی بین اتم های نیتروژن و هیدروژن ایجاد می شود. با مقایسه دو اتم نیتروژن در مولکول هیدرازین، می توان به این نکته اشاره کرد که این ترکیب شیمیایی دارای تعدادی اتم های هیدروژن و همچنین جفت های تک الکترون می باشد.
با این حال، اتم های هیدروژن متصل به یک اتم نیتروژن در صفحه عمودی قرار می گیرند، در حالی که اتم های هیدروژن متصل به اتم نیتروژن دیگر در صفحه افقی قرار می گیرند. این ساختار منجر به ایجاد گشتاور دو قطبی خالص در مولکول هیدرازین می شود.
ویژگی های هیدرازین چیست؟
- فرمول شیمیایی: N۲H۴
- رنگ: بی رنگ
- ظاهر: دودی به شکل مایع روغنی
- وزن مولکولی: ۳۲.۰۴۵۲ گرم در مول
- تراکم : ۱.۰۲۱ گرم بر سانتی متر مکعب
- نقطه جوش : ۱۱۴ درجه سانتی گراد
- نقطه ذوب: ۲ درجه سانتی گراد
- هیبریداسیون: sp 3
- زاویه باند: ۱۰۹.۵ درجه
- انحلال پذیری: قابل امتزاج در آب
- ضریب شکست: ۱.۴۶۰۴۴
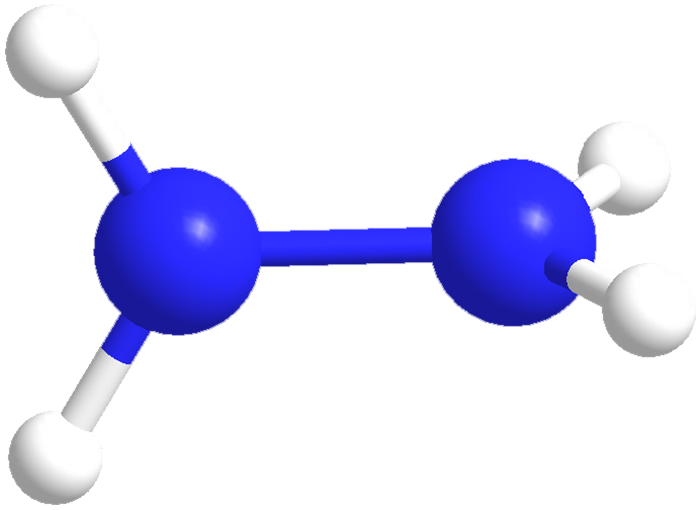
هیدرازین چینی ۵۵%
روش های سنتز هیدرازین
فرآیند تولید این ترکیب شیمیایی برای اولین بار در سال ۱۹۰۶ از واکنش NaOCl با NH۳ به صورت صنعتی انجام شد. هیدرازین به دست آمده با این روش یک محلول آبی رقیق ۱٪ – ۲٪ است و میزان سنتز کل حدود ۶۷٪ است. مقدار قابل توجهی گرما برای استخراج هیدرات هیدرازین از محلول رقیق مورد نیاز است و به ازای هر ۱ کیلوگرم هیدرات هیدرازین بازیابی شده، ۴۰ تا ۱۱۰ کیلوگرم آب مورد نیاز است. به دلیل استفاده بیش از حد از آمونیاک، لازم است دستگاه بازیابی اضافه شود که در کنار هم مقدار زیادی NaCl و NH۴Cl و سایر نمک ها تولید می شود. وجود واکنش های جانبی باعث کاهش بازده تولید هیدرازین می شود.
به منظور کاهش واکنش های جانبی، معمولا مقدار زیادی آمونیاک خام مصرف می شود، به طوری که هیدرازین همیشه در غلظت های پایین (۱٪ -۲٪ وزنی) در محلول واکنش قرار دارد. در نتیجه مقدار زیادی آب آمونیاکی نیاز به جداسازی و بازیافت دارد و تقطیر هیدرازین باعث مصرف بخار بیشتری می شود.
امروزه فرآیندهای متنوعی برای سنتز هیدرازین ایجاد شده است. از بین فرآیندهای زیادی که در طی یک دوره زمانی توسعه یافته اند، آنها به طور کلی به دو بخش عمده طبقه بندی می شوند. روش های سنتز هیدرازین عبارتند از:
اکسیداسیون آمونیاک
این ترکیب شیمیایی از واکنش آمونیاک با پراکسید هیدروژن در حضور یک کاتالیزور کتون ایجاد می شود. این روشی است که به نام فرآیند پراکسید شناخته می شود. گاهی اوقات به آن فرآیند Pechiney y-Ugine-Kuhlmann، چرخه Atofina-PCUK یا فرآیند کتازین نیز گفته می شود. مراحل انجام واکنش به شرح زیر است:
NH۳ + H۲O۲ → N۲H۴ + ۲H۲O2
در این مسیر ابتدا ایمین از تراکم کتون و آمونیاک تولید میشود که سپس توسط پراکسید هیدروژن اکسید می شود تا هیدرازین تولید شود. این فرآیند منجر به تشکیل یک پیوند نیتروژن واحد می شود؛ بنابراین هیدرازون با یک یا چند معادل از کتون متراکم می شود.
اکسیداسیون های مبتنی بر کلر
هیپوکلریت سدیم که یک ماده فعال است که در بسیاری از فرآیندها استفاده می شود. فرآیند واکنش هیپوکلریت سدیم با آمونیاک به فرآیند Olin Raschig معروف است که اولین بار در سال ۱۹۰۷ معرفی شد. این روش به واکنش مونو کلرو آمین با آمونیاک بستگی دارد که پیوند واحد نیتروژن- نیتروژن را با HCl به عنوان محصول جانبی ایجاد می کند. واکنش به شرح زیر است:
NH۲Cl + NH۳ → H۲NNH۲ + HCl
در فرآیند فوق، اوره نیز می تواند به جای آمونیاک اکسید شود. در مورد اوره نیز، هیپوکلریت سدیم به عنوان یک آنتی اکسیدان عمل می کند. این فرآیند عمدتا در آسیا انجام می شود، زیرا مقدار قابل توجهی محصولات جانبی تولید می کند.
بهبود تکنیکال روش سنتز هیدرازین
در سال های اخیر، هدف از بهبود فرآیندهای تولید این ماده شیمیایی پرکاربرد، مهار واکنش جانبی و افزایش بازده تولید در صنایع شیمیایی بوده است. مواد افزودنی مختلفی را مانند KMnO۴ و MnSO۴می توان برای بهبود تولید و کاهش واکنش های جانبی به محیط واکنش اضافه کرد. این دو ترکیب شیمیایی به طور گسترده در کشور چین برای تولید هیدرازین استفاده می شوند.
با این حال، این دو افزودنی در محلول اوره به راحتی حل می شوند و رنگ قرمز تیره را ایجاد می کنند؛ بنابراین کنترل دقیق آنها در عملکرد واقعی می تواند بسیار دشوار باشد. در عین حال در اثر واکنش نمک منگنز، اکسید منگنز تولید می شود که می تواند منجر به پوسته پوسته شدن لوله های واحد تولید و حتی مسدود شدن آن ها شود. اکسید منگنز ممکن است باعث آلودگی محیط زیست نیز شود؛ بنابراین برای جایگزینی آن از ترکیبات دیگری مانند سولفات منیزیم استفاده می شود.
عوارض و خطرات هیدرازین چیست؟
این ماذه شیمیایی از طریق تماس پوستی، تماس چشمی، استنشاق و بلع باعث عوارض می شود. قرار گرفتن در معرض این ماده می تواند باعث سوزش پوست، درماتیت تماسی، سوزش چشم، بینی، گلو، حالت تهوع و استفراغ، تنگی نفس، مشکل ریوی، سردرد، سرگیجه، کاهش فعالیت سیستم عصبی مرکزی، بی حالی، کوری موقت، تشنج و اغما شود.
قرار گرفتن در معرض این ماده همچنین می تواند باعث آسیب اعضای بدن از جمله کبد، کلیه ها و سیستم عصبی مرکزی شود.
افزایش بروز تومورهای ریه و کبد در موشهایی که در معرض هیدرازین قرار گرفته اند در آزمایشات مشاهده شده است. همچنین موش ها و همسترهایی که از طریق آب آشامیدنی، استنشاق، گاواژ و تزریق در معرض این ماده قرار گرفتند دچار تومورهای داخل حفره بینی شدند.
قرار گرفتن در معرض مقادیر کم هیدرازین از طریق دود دخانیات نیز امکان پذیر است و در حال حاضر اطلاعات کافی در مورد اثرات سرطان زای این ماده در انسان در دسترس نیست.
محصولات مشابه

انیدرید مالئیک چینی و کره ای و تایوانی

پلی الکترولیت کاتیونی و آنیونی

سولفات مس یا کات کبود

اسید اگزالیک چینی

کلسیم کلراید خوراکی و صنعتی

کلر ژاپنی نای کلن و استارکلن

کربنات پتاسیم و هیدروکسید پتاسیم

